Sisik dan Sirip Ikan
Sisik dan sirip ikan merupakan limbah yang banyak dihasilkan dari hasil pengolahan ikan yang hanya terbuang begitu saja, sehingga dapat mencemari lingkungan. Selain itu, tulang ikan juga merupakan salah satu limbah dari industri perikanan yang belum dimanfaatkan dengan baik. Tulang ikan terdiri dari senyawa organik dan senyawa anorganik (mineral). Menurut Jung et al. (2005) dalam Putranto et al. (2015), tulang ikan hoki (Johnius belengerii) mengandung bahan organik sekitar 30,54% (bk) yang terdiri dari protein 28,04%, lipid 1,94% dan karbohidrat 0,56%, sedangkan bahan mineral anorganiknya sekitar 69,46% (bk) terutama terdiri dari 59,69% kalsium (Ca) dan 35,81% fosfor (P).
Kalsium merupakan unsur utama yang diperlukan untuk pertumbuhan dan berfungsinya ujung-ujung akar. Kalsium di dalam tanaman sangat penting untuk menetralisasi senyawa asam. Senyawa asam ini bila konsentrasinya terlalu tinggi, mempunyai pengaruh negatif terhadap tumbuhan. Untuk struktur tanah pertanian sangat penting, bahwa kompleks adsorpsi ion-ion Ca2+ di dalam air tanah harus cukup tinggi. Kalsium dari tulang ikan memiliki kualitas cukup bagus serta mudah diperoleh. Salah satu pemanfaatan tulang ikan, yaitu pengolahan menjadi tepung tulang. Pemanfaatan tepung tulang dapat dijadikan suplemen dan obat pencegah osteoporosis (Jiancong et al., 2010 dalam Putranto et al., 2015). Selain itu, tepung tulang dapat juga dimanfaatkan dalam pembuatan mie kering (Mulia, 2004 dalam Putranto et al., 2015).
Proses Pengolahan
Sampel sisik dan sirip ikan mujair diambil dari limbah hasil buangan ikan yang tidak digunakan lagi hanya dibiarkan menumpuk dan membusuk begitu saja di pasar penjualan ikan mujair (Oreochromis mosambicus) yang terletak di jalan Towua Palu. Ikan mujair yang dijual berasal dari danau Lindu Sulawesi Tengah. Pada proses jual beli berlangsung ikan langsung dibersihkan di tempat tersebut, dimana yang dibuang sebagai limbah, yaitu sisik, sirip, ekor, dan isi perut ikan. Dari hasil buangan tersebut limbah yang diambil untuk dianalisis dalam penelitian ini adalah sisik dan sirip ikan mujair. Limbah yang diambil ± 500 gram, kemudian dilakukan analisis.
Sampel limbah sisik dan sirip ikan mujair yang telah diambil, dicuci bersih kemudian ditiriskan dan dikeringkan tanpa matahari diangin-anginkan pada suhu kamar, kemudian dimasukkan ke dalam cawan penguap dan ditimbang sebanyak 100 gram, lalu dipanaskan dalam oven pada suhu 105oC selama ± 3 jam. Setelah itu didinginkan dalam desikator dan ditimbang. Kemudian ditentukan kadar airnya dengan rumus kadar air (Sudarmadji et al., 1989 dalam Tiwow et al., 2016).
Sampel limbah sisik dan sirip ikan mujair kering ditimbang diperoleh, yaitu sisik sebesar 79,54 gram dan sirip sebesar 74,37 gram, lalu sampel limbah sisik dan sirip ikan mujair kering diabukan dalam tanur pada suhu 700oC selama ± 3 jam. Kemudian abu yang diperoleh ditimbang dan ditentukan kadar abunya dengan rumus kadar abu (Sudarmadji et al., 1989 dalam Tiwow et al., 2016).
Menimbang sampel abu sisik dan sirip ikan mujair, yaitu masing-masing sebanyak 15 gram. Kemudian menambahkan larutan HNO3 pekat sebanyak 20 mL ke dalam masing-masing sampel, kemudian disaring, hingga terpisah antara filtrat dan residu. Dalam penelitian ini yang diambil hanyalah filtratnya saja sedangkan residunya tidak digunakan. Filtrat yang diperoleh selanjutnya diencerkan dengan aquades dalam labu ukur 100 mL sampai tanda batas.
Larutan sampel yang sudah siap untuk dianalisis dimasukkan ke dalam vial (tempat sampel berukuran 10 mL yang bentuknya menyerupai botol). Analisis kadar Ca pada sampel sisik dan sirip ikan mujair dilakukan dengan cara memasukkan masing-masing 10 mL sampel ke dalam vial, dimana untuk sampel sisik ikan mujair ke dalam 3 buah vial dan sampel sirip ikan mujair juga ke dalam 3 buah vial dan menambahkan reagen (pereaksi) Ca, yaitu metil petaline (C20H26NO3) ke dalam masing-masing vial tersebut, kemudian dikocok sampai pereaksi larut semua menjadi homogen dan larutan berubah warna dari bening menjadi warna merah muda.
Alat yang digunakan dalam penelitian sisik dan sirip ikan adalah neraca digital ARC-120, oven MMM Medcenter, tanur FB1410M, dan spektrofotometer Spektro Direct RS232 serial No: 1257060900344. Bahan yang digunakan dalam penelitian ini adalah limbah sisik dan sirip ikan mujair (Oreochromis mossambicus), aquades, larutan HNO3 pekat (Merck), reagen phosphate 1 dan 2 (Livobond) dan reagen metil petaline (C20H26NO3) (Livobond).
Proses pengolahan tepung tulang merupakan modifikasi dari metode yang telah dilakukan oleh Trilaksani (2006) dalam Putranto et al. (2015). Proses pengolahan tulang dalam penelitian ini adalah sebagai berikut:
a. Pencucian
Tulang ikan belida (Chitala sp.) dalam kondisi beku dilelehkan dengan air mengalir. Selanjutnya tulang dicuci dan ditiriskan.
b. Perebusan tulang
Tulang yang diambil dari limbah pengolahan amplang dimasukkan ke dalam panci aluminium pada saat suhu air mencapai 80°C. Tulang direbus selama 30 menit. Perebusan awal ini dilakukan untuk mempermudah pembersihan tulang dari daging, darah dan lemak yang masih menempel pada tulang.
c. Pembersihan
Tulang yang telah direbus kemudian dicuci dengan air bersih untuk menghilangkan daging-daging ikan yang masih menempel pada tulang sampai cukup bersih. Selanjutnya tulang yang telah bersih ditiriskan dan ditimbang sebanyak 200 gram untuk setiap perlakuan.
d. Proses Presto
Proses presto merupakan proses pemasakan menggunakan panci bertekanan yang dapat mempercepat lama waktu pemasakan dibanding tanpa menggunakan panci presto. Proses presto ini berfungsi untuk menghilangkan lemak yang terdapat pada tulang serta mendenaturasi protein. Selain itu, proses presto juga bertujuan untuk mengempukkan tulang ikan sehingga mempermudah proses penepungan. Tulang ikan belida (Chitala sp.) yang telah ditimbang (200 gram), selanjutnya dilakukan proses presto (P) dengan dua perlakuan lama presto yaitu 2 jam (P2) dan 3 jam (P3).
e. Proses perebusan
Proses perebusan merupakan kelanjutan perlakuan dari penelitian tersebut. Setelah tulang ikan di presto sesuai perlakuan, maka dilanjutkan dengan proses perebusan (R) dengan dua perlakuan frekuensi perebusan, yaitu perebusan 1 kali (R1) dan perebusan 2 kali (R2) dengan lama perebusan untuk setiap frekuensi perebusan selama 30 menit. Perebusan tulang dilakukan dengan cara mendidihkan 2 liter air dalam panci aluminium dengan suhu 100°C. Selanjutnya, tulang ikan dimasukkan dan dibiarkan selama 30 menit. Setelah direbus selama 30 menit, tulang ikan segera diangkat dan ditiriskan (R1). Sedangkan pada perlakuan 2 kali proses perebusan (R2), setelah proses perebusan pada perlakuan R1 dilanjutkan proses perebusan kedua dengan cara mengganti air perebusan pertama dan direbus dengan cara seperti pada perlakuan R1. Tulang yang telah menjalani perebusan selama 2 kali, selanjutnya ditiriskan.
f. Ekstraksi Basa NaOH
Proses ektraksi basa NaOH adalah proses perendamanan tulang di dalam larutan NaOH 1,5 N selama 2 jam pada suhu 60°C untuk masing-masing perlakuan. Proses ini bertujuan untuk menghilangkan protein. g. Pencucian Tulang ikan ditempatkan pada kain saring selanjutnya dibilas menggunakan air mengalir. Proses ini beryujuan untuk menetralkan pH tulang ikan.
h. Pengeringan
Tulang ikan belida (Chitala sp.) selanjutnya diletakkan di atas tray yang telah dilapisi terlebih dahulu dengan lembaran aluminium foil. Tulang tersebut dikeringkan menggunakan oven pengering selama 48 jam pada suhu 65°C.
Penepungan
Tepung tulang yang telah kering dihaluskan menggunakan blender dan diayak menggunakan ayakan tepung. Rancangan Percobaan Penelitian ini menggunakan rancangan acak lengkap, terdiri dari 4 perlakuan dan 3 ulangan yaitu P2R1 (lama presto 2 jam, frekuensi perebusan 1 kali), P2R2 (lama presto 2 jam, frekuensi perebusan 2 kali), P3R1 (lama presto 3 jam, frekuensi perebusan 1 kali), dan P3R2 (lama presto 3 jam, frekuensi perebusan 2 kali).
Analisis Data
Data dianalisis keragamannya (ANOVA), dan bila hasilnya menunjukkan ada beda nyata, dilanjutkan uji Beda Nyata Terkecil (BNT) pada selang kepercayaan 95% aplikasi Minitab® 17.1.0. Prosedur analisis perhitungan kadar kalsium dilakukan menggunakan metode titrasi permanganometri berdasarkan Sudarmadji (1984) dalam Putranto et al. (2015).
Kandungan Kalsium
Hasil pengukuran yang diperoleh menggunakan alat Spectro Direct, konsentrasi Ca dalam ikan mujair (Oreochromis mossambicus) berupa konsentrasi logam dalam larutan sampel (mg/L). Selanjutnya konversi konsentrasi logam dalam larutan sampel (ppm) menjadi konsentrasi logam berat kering sampel (mg/kg) dengan menggunakan persamaan berikut: Y = V . X / m dimana: Y = Kadar Ca dalam sampel (mg/kg); V = Volume penetapan sampel (L); X = Konsentrasi larutan sampel (mg/L); m = Berat sampel kering (kg) (Sudarmadji et al., 1989 dalam Tiwow et al., 2016).
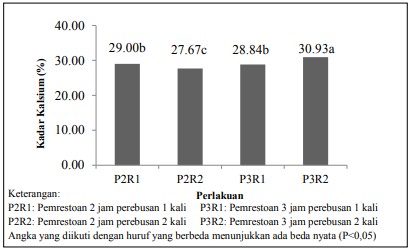
Kalsium merupakan unsur kelima dan kation terbanyak di dalam tubuh, yaitu 1,5-2% dari seluruh tubuh. Lebih dari 99% kalsium terdapat di dalam tulang rawan dan gigi, sisanya di dalam cairan tubuh dan jaringan lunak (Nasoetion et al., 1995 dalam Putranto et al., 2015). Hasil pengamatan kadar kalsium tepung tulang ikan belida disajikan pada Gambar 1.
Gambar 1. Histogram lama waktu proses presto dan frekuensi perebusan terhadap kadar kalsium tepung tulang ikan belida
Kadar kalsium yang diperoleh sedikit lebih rendah dibanding dengan kadar kalsium tepung tulang ikan tuna sebesar 39,24% hasil penelitian Trilaksani (2006) dalam Putranto et al. (2015. Standar Nasional Indonesia (SNI 01- 3158-1992) kadar kalsium untuk tepung tulang ikan ditetapkan untuk mutu I adalah 30% bb dan mutu II sebesar 20% bb. Merujuk dari standar tersebut, maka kadar kalsium tepung tulang ikan belida hasil penelitian ini termasuk ke dalam mutu I dan mutu II.
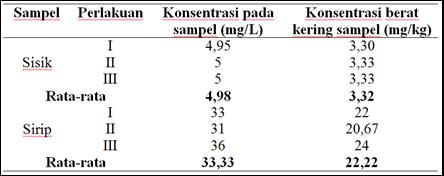
Gambar 2. Data kadar Ca dalam sampel limbah sisik dan sirip ikan mujair
Hasil yang diperoleh dari penelitian ini adalah konsentrasi Ca dalam sampel sisik ikan mujair dengan nilai rata-rata yaitu 4,98 mg/L dengan konsentrasi berat kering sampel diperoleh nilai rata-rata yaitu 3,32 mg/kg. Sedangkan dalam sirip ikan diperoleh nilai rata-rata yaitu 33,33 mg/L dengan konsentrasi berat kering sampel diperoleh nilai rata-rata 22,22 mg/kg. Konsentrasi P dalam sampel sisik ikan mujair diperoleh nilai rata-rata yaitu 73,33 mg/L dengan konsentrasi berat kering sampel diperoleh nilai rata-rata yaitu 48,88 mg/kg. Sedangkan dalam sirip ikan diperoleh nilai rata-rata yaitu 145,33 mg/L dengan konsentrasi berat kering sampel diperoleh nilai rata-rata yaitu 96,88 mg/kg. Hasil penelitian menunjukkan bahwa kandungan kalsium terbanyak terdapat pada sirip ikan mujair, yaitu dengan konsentrasi sampel rata-rata yaitu 33,33 mg/L dan konsentrasi berat kering sampel rata-rata 22,22 mg/kg.
DAFTAR PUSTAKA
Putranto, H. F., A. N. Asikin dan I. Kusumaningrum. 2015. Karakterisasi tepung tulang ikan belida (Chitala sp.) sebagai sumber kalsium dengan metode hidrolisis protein. Ziraa’ah. 40 (1): 11-20.
Tiwow, V. M. A., I. W. Hafid dan Supriadi. 2016. Analisis kadar kalsium (Ca) dan fosforus (P) pada limbah sisik dan sirip ikan mujair (Oreochromis mossambicus) dari Danau Lindu Sulawesi Tengah. J. Akad. Kim. 5 (4): 159-165.

Comments
Post a Comment